Inflamação crônica e reparo tecidual: fundamentos e implicações clínicas
A inflamação é um mecanismo fundamental de defesa do organismo frente a diferentes formas de agressão, como infecções, traumas, agentes químicos, corpos estranhos e necrose tecidual. Mas quando se torna persistente, a inflamação crônica compromete diretamente o reparo tecidual.
Entender essa transição é vital para o manejo clínico e cirúrgico. Continue a leitura para entender as bases moleculares e as implicações desse processo.
Conceitos gerais sobre inflamação
A inflamação pode ser definida como uma resposta dos tecidos vascularizados a uma agressão, caracterizada por alterações vasculares, recrutamento de células inflamatórias e liberação de mediadores químicos. Classicamente, é descrita pelos sinais cardinais: rubor, calor, tumor e dor.
Trata-se de uma resposta complexa, coordenada por mediadores celulares e moleculares, cujo objetivo inicial é eliminar o agente agressor e iniciar o processo de reparo. Em condições ideais, a inflamação é autolimitada e culmina na restauração da homeostase tecidual.
No entanto, quando esse processo se torna persistente ou desregulado, estabelece-se a inflamação crônica, condição intimamente associada a falhas no reparo tecidual, fibrose excessiva e diversas doenças clínicas e cirúrgicas.
Fatores que interferem na cicatrização
Além dos mecanismos intrínsecos da resposta inflamatória, diversos fatores sistêmicos e locais podem interferir negativamente no processo de cicatrização.
Condições como desnutrição proteico-calórica, deficiência de micronutrientes (especialmente zinco, ferro e vitaminas A e C), diabetes mellitus, obesidade, tabagismo, insuficiência vascular e uso crônico de corticosteroides estão associadas a atraso no reparo tecidual e maior risco de complicações.
No diabetes mellitus, por exemplo, a hiperglicemia crônica compromete a função dos neutrófilos e macrófagos, reduz a angiogênese e favorece um estado inflamatório persistente.
A obesidade, por sua vez, associa-se à hipóxia tecidual relativa, aumento de citocinas pró-inflamatórias e maior risco de infecção. Esses fatores devem sempre ser considerados na avaliação clínica, pois a correção das condições sistêmicas é parte fundamental do sucesso do reparo tecidual.
Diferenças entre inflamação aguda e inflamação crônica
Do ponto de vista fisiopatológico, a inflamação é tradicionalmente dividida em inflamação aguda e inflamação crônica.
A inflamação aguda caracteriza-se por início rápido, curta duração e predomínio de neutrófilos, sendo típica de infecções bacterianas, traumas e necrose tecidual.
Já a inflamação crônica apresenta curso prolongado, com predomínio de macrófagos, linfócitos e plasmócitos, além de intensa remodelação tecidual, angiogênese e fibrose.
Na inflamação crônica, o estímulo inflamatório persiste ou o mecanismo de resolução falha. Isso pode ocorrer por infecções persistentes, exposição contínua a agentes tóxicos, doenças autoimunes ou resposta inflamatória desregulada.
Diferentemente da inflamação aguda, que prepara o terreno para o reparo, a inflamação crônica frequentemente interfere negativamente na regeneração tecidual.
Bases celulares e moleculares da inflamação crônica
Os macrófagos desempenham papel central na inflamação crônica. Derivados dos monócitos circulantes ou residentes nos tecidos, essas células atuam como fagócitos, células apresentadoras de antígeno e importantes fontes de citocinas, fatores de crescimento e mediadores inflamatórios.
Dependendo do microambiente, os macrófagos podem assumir fenótipos pró-inflamatórios (M1) ou anti-inflamatórios e reparadores (M2).
Na inflamação crônica, observa-se frequentemente um desequilíbrio entre esses fenótipos, com manutenção de sinais pró-inflamatórios, produção sustentada de citocinas como TNF-α, IL-1β e IL-6, e ativação contínua de vias de sinalização intracelular, como NF-κB e STAT.
Esse ambiente perpetua o recrutamento celular e interfere na transição adequada para a fase de reparo.
Além dos macrófagos, linfócitos T e B participam ativamente da inflamação crônica, especialmente em doenças autoimunes. A interação entre imunidade inata e adaptativa contribui para a persistência da inflamação e para o dano tecidual progressivo.
Reparo tecidual: princípios fundamentais
O reparo tecidual é o conjunto de processos que visam restaurar a integridade estrutural e funcional de um tecido após lesão.
Esse processo pode ocorrer por regeneração, quando há reposição das células perdidas por células idênticas, ou por cicatrização, quando o tecido original é substituído por tecido fibroso.
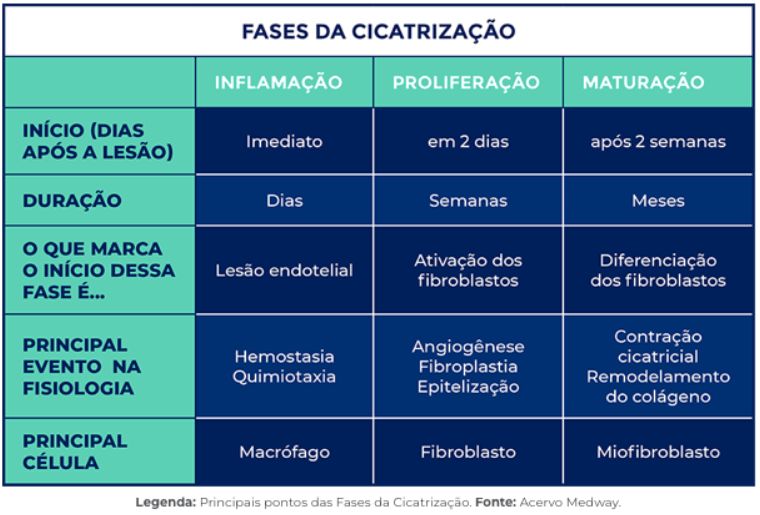
Classicamente, o reparo tecidual é dividido em fases sobrepostas: hemostasia, inflamação, proliferação e remodelamento:
Hemostasia
A hemostasia ocorre imediatamente após a lesão, com formação do coágulo de fibrina, que atua como matriz provisória e fonte de mediadores inflamatórios.
Inflamatória
Em seguida, a fase inflamatória promove a remoção de debris celulares e patógenos, preparando o leito da ferida.
Proliferativa
A fase proliferativa é marcada pela formação do tecido de granulação, angiogênese, proliferação de fibroblastos e deposição inicial de matriz extracelular.
Remodelamento
Por fim, a fase de remodelamento pode durar semanas a anos, com reorganização das fibras colágenas, redução da vascularização e aumento da resistência tênsil da cicatriz.
Relação entre inflamação crônica e falha no reparo
A resolução adequada da inflamação é um pré-requisito essencial para o reparo eficiente. Quando a inflamação persiste, ocorre prejuízo direto em várias etapas do processo cicatricial.
A produção contínua de citocinas pró-inflamatórias e espécies reativas de oxigênio pode levar à degradação excessiva da matriz extracelular, apoptose celular e disfunção dos fibroblastos.
Em feridas crônicas, como úlceras venosas, úlceras diabéticas e lesões por pressão, observa-se um estado inflamatório persistente, frequentemente associado à infecção, isquemia e hipóxia tecidual.
Nesses cenários, há redução da resposta angiogênica efetiva, comprometimento da migração celular e incapacidade de progressão para a fase de remodelamento.
Além disso, a inflamação crônica pode resultar em fibrose patológica. A ativação prolongada de fibroblastos e miofibroblastos leva à deposição excessiva de colágeno e outros componentes da matriz extracelular, culminando em perda da arquitetura normal do tecido e comprometimento funcional, como o observado em queloides.
Implicações clínicas da inflamação crônica no reparo tecidual
Do ponto de vista clínico, a compreensão da inflamação crônica tem implicações diretas na abordagem de múltiplas condições. Em cirurgia, a presença de inflamação crônica está associada a maior risco de deiscência de suturas, infecção de ferida operatória e cicatrização inadequada.
Na prática clínica, estratégias terapêuticas modernas buscam não apenas controlar a infecção ou remover o tecido desvitalizado, mas também modular a resposta inflamatória.
O controle glicêmico rigoroso, a otimização da perfusão tecidual, o manejo da carga bacteriana e o uso racional de curativos avançados são exemplos de intervenções baseadas nesses princípios.
Além disso, avanços na biologia molecular e na engenharia de tecidos têm permitido o desenvolvimento de terapias inovadoras, como o uso de fatores de crescimento, matrizes extracelulares acelulares, terapias celulares e biomateriais, com o objetivo de restaurar um microambiente favorável ao reparo.
Conclusão
A inflamação crônica representa um dos principais obstáculos ao reparo tecidual eficaz. Embora a inflamação seja essencial para a defesa do organismo e para o início da cicatrização, sua persistência resulta em dano tecidual progressivo, fibrose e falha na regeneração.
Para o médico, reconhecer os mecanismos envolvidos nesse processo é fundamental para a tomada de decisões clínicas e cirúrgicas mais adequadas.
O entendimento integrado entre inflamação, reparo tecidual e contexto clínico permite uma abordagem mais racional e eficaz das doenças inflamatórias crônicas e das feridas de difícil cicatrização.
À medida que novas terapias moduladoras da inflamação e estratégias de reparo avançado se desenvolvem, torna-se cada vez mais importante que o profissional de saúde domine esses conceitos.
Entender a fisiopatologia é o primeiro passo para um diagnóstico preciso e um tratamento eficaz. No Blog da Medway, você encontra guias práticos e atualizações essenciais para sua carreira médica e preparação para a residência.
Referências
Kumar V, Abbas AK, Aster JC. Robbins & Cotran – Pathologic Basis of Disease. Elsevier.
Sen CK, Roy S. Cicatrização de feridas. In: Neligan PC et al. Cirurgia Plástica. Elsevier.
Eming SA, Martin P, Tomic-Canic M. Wound repair and regeneration: mechanisms, signaling, and translation. Science Translational Medicine.

Lizandra Rener Cavioli
Médica pela Universidade Federal do Triângulo Mineiro com residência em Cirurgia Geral pela Unifesp.




